搜尋結果
以下是含有上市許可的搜尋結果,共276筆
-
仁新Belite新藥 英國可望取證
仁新(6696)3日宣布,美國子公司Belite Bio(那斯達克代碼:BLTE)獲英國藥品與醫療產品監管署(MHRA)同意可依據治療青少年斯特格病變(STGD1)新藥LBS-008第三期臨床試驗「DRAGON」的期中結果,提交條件式上市許可(CMA)申請,有機會拿下全球首款治療此罕見眼疾藥物的藥證。
-
《興櫃股》仁新獲英核准以LBS-008期中分析 提交條件式上市許可申請
仁新(6696)子公司Belite Bio, Inc(那斯達克股票交易代碼:BLTE,以下簡稱Belite)宣布,英國藥品與醫療產品監管署(MHRA)同意基於LBS-008(Tinlarebant)治療青少年斯特格病變(STGD1)臨床三期試驗DRAGON之期中分析結果,Belite可提交STGD1條件式上市許可(Conditional Marketing Authorization, CMA)申請。
-
《興櫃股》泰合抗血栓口溶膜 申請歐盟上市許可
泰合(6467)宣布,已於中歐時間10月30日正式向歐洲藥品管理局(EMA)提交TAH3311的歐洲上市許可申請。此項申請標誌著泰合生技在推動產品進軍歐洲市場及深化全球佈局上的重要里程碑。
-
全球首款Apixaban口溶膜劑型 泰合抗凝血藥 進軍歐洲
泰合(6467)宣布,已於中歐時間10月30日向歐洲藥品管理局(EMA)提交旗下新藥TAH3311的歐洲上市許可申請,此為全球首款Apixaban口溶膜劑型,象徵公司產品正式進軍歐洲市場,並在全球抗凝血用藥領域邁出重要一步。
-
太景新藥 插旗印度市場
太景*-KY(4157)宣布,旗下抗病毒新藥Pixavir marboxil(TG-1000)與印度藥廠簽署商業化授權協議,太景全球藥品版圖正式進入南亞藥品市場。此項合約內容授權抗感染新藥於印度的開發及銷售權,由印度合作夥伴負責授權區域內的開發、上市許可申請、藥品製造及市場銷售等項目;依據合約,太景將有簽約金、里程碑款及銷售權利金收入。
-
《生醫股》太景新藥TG-1000授權印度藥廠 拓展南亞市場
新藥研發公司太景*-KY(4157)旗下抗病毒新藥Pixavir marboxil(TG-1000)與印度藥廠簽署商業化授權協議,太景全球藥品版圖正式進入南亞藥品市場。
-
中裕Trogarzo 獲沙國授權
中裕(4147)20日宣布,旗下創新抗體藥物Trogarzo(ibalizumab-uiyk),再獲沙烏地阿拉伯食藥局(SFDA)授予罕見疾病藥物資格(Orphan Drug Designation),用於治療對多重抗藥性HIV-1感染且現行抗病毒療法失敗的重度治療經驗型成人患者。
-
《生醫股》中裕愛滋病新藥獲SFDA罕見疾病藥物資格 股價平盤震盪
中裕(4147)愛滋病新藥獲沙烏地阿拉伯食品藥品管理局(SFDA)授予罕見疾病藥物資格,今(20)日股價跳空開高,晨盤開高後,多空在平盤處展開攻防。
-
《生醫股》ABC-KY Q3營收連5季成長 前3季超越去年全年
瑞磁生技ABC-KY(6598)2025(今)9月營收4447萬元,年成長139.58%,第三季營收達1.2億元,年增率亦達64%,創下連五季成長紀錄;前三季累積營收達新台幣3.6億元,已超越去年全年營收的3.4億元。
-
《生醫股》PTS302出貨暢旺 共信-KY9月營收續創新高
共信-KY(6617)受惠中國大陸醫院通路布建效益顯現,肺癌新藥普羅先安(PTS302)出貨暢旺,帶動9月合併營收達新台幣505萬元,續創歷史新高,月增17.17%、年增82.24%;前3季合併營收2,854萬元,年增19.28%,同步改寫新高紀錄。若以功能性貨幣美元衡量,9月及累計前三季營收亦維持成長趨勢,顯示營運處於持續上升軌道。
-
太景簽新藥授權協議 正式進軍越南
太景*-KY(4157)1日公告,子公司太景生技與越南藥廠Fideschem Inc.及Newsun Pharmaceutical JSC.,簽署抗生素新藥太捷信於越南的授權合約,繼星馬之後,再一步拓展東南亞藥品市場。
-
台康生 新藥開發利多
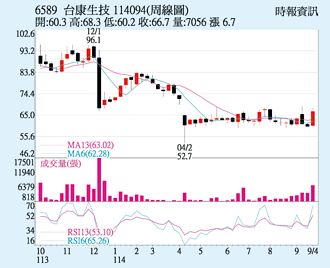
台康生(6589)受惠乳癌生物相似藥EG1206A,獲美國FDA及歐盟EMA同意豁免進行臨床三期試驗,將可直接加速推進該產品的全球上市許可申請(BLA/MAA),26日逆勢上漲6.04%,以66.7元創下近二個月波段新高,成交量放大至4,216張,技術面翻多,外資連二買,有利多頭。
-
《生醫股》省經費+時間 台康乳癌生物相似藥豁免進行臨床三期試驗
台康生技(6589)與美國食品藥物管理局(FDA)及歐盟藥品管理局(EMA)進行科學諮詢正在進行開發乳癌生物相似藥產品EG1206A(Pertuzumab biosimilar)三期臨床試驗豁免得到正面回應,也正式終止EG1206A的三期臨床試驗。這項豁免臨床三期試驗成果,台康將加速送審資料準備,產品進入市場的時間也會縮短。
-
年收入估逾5億 台睿啖保健品市場大餅
台睿(6580)23日宣布進軍保健品市場,首推「硒2皙煥白膜衣錠」。台睿董事長林群表示,預計保健品可為台睿每年創造5億元以上的收入,再配合公司新藥的技轉方案推動,將展現多年投研發成果收穫,助力明年的上市規劃。
-
製藥俠客陳正 面臨健亞被收購危機
1993年陳正辭去美國諾華藥廠的工作,舉家返台與矽谷創投大老孔繁建攜手,在國發基金支持下成立健亞(4130),成為台灣最早一批「海歸派」新藥創業者。不過這位充滿理想的製藥業俠客,卻正面臨健喬(4114)將公開收購的考驗。
-
《生醫股》安克三箭齊發 布局AI醫療新藍海
安克(4188)今(2)日下午舉行法說會,營運三大亮點策略包括,「安克甲狀偵」推進健保沙盒計、擴大「安克呼止偵」在台的醫院滲透率,下半年持續推動國際市場落地、掌握One-Device AI超音波診斷趨勢,積極推動結合AI的掌上型超音波(POCUS)市場新藍海。
-
禾榮科總經理沈孝廉 笑臉管理 率年輕隊打拚
禾榮科總經理沈孝廉為財務背景出身,曾經擔任漢微科財務長的他,於2019年正式完成與ASML整合任務後回到漢民集團,並在董事長黃民奇邀請下,便投身到禾榮科,負責與工研院、清大AB-BNCT(硼中子捕獲治療)技術轉移發展,從財務、半導體設備,再到生技醫療設備產業,橫跨領域多元。
-
逸達前列腺癌新藥 獲美FDA上市許可
逸達26日公告,旗下治療前列腺癌新劑型新藥CAMCEVI三個月劑型,通過美國FDA上市審查,由於後續還須取得J-Code等流程,預期正式上市並貢獻營收會落在今年底。該藥由授權夥伴Intas美國子公司Accord負責市場銷售,逸達在取證與藥品正式上市時,都有機會取得里程碑金,未來並有銷售分潤。
-
罕病AADC基因治療「價格近億」納健保 首年13人受惠
AADC缺乏症是一種遺傳性罕見疾病,通常在嬰兒早期出現症狀。由台大醫院團隊研發的AADC基因治療,2022年獲歐盟上市許可,價格近億元。健保署藥物共擬會今天(21)審查通過健保給付,將和廠商啟動價量協議,預計今年12月1日生效,預估第一年13名患者受惠。
-
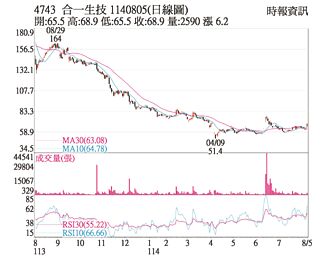
熱門股-合一 KD指標翻多向上
合一(4743)新藥Fespixon海外藥證持續報喜,而乳膏Bonvadis亦獲FDA核准用於全皮層慢性傷口適應症的美國上市許可,預期將助力業績成長,5日買盤強勁,股價收漲停板68.9元改寫一個多月新高,KD指標翻多向上,成交量2,556張。