搜寻结果
以下是含有孤儿药的搜寻结果,共147笔
-
益安、台宝、三鼎 抢滩美国
不让新药业专美于前,再生医疗与创新医材10月亦报佳音,益安(6499)、台宝(6892)、三鼎(6808)抢滩美国市场,法人指出,除了产品商业化外,加速跨国临床合作与海外设厂已成趋势。
-
《生医股》药华药Ropeg申请美国ET药证 力拚2026取证
药华药(6446)今(31)日宣布,正式向美国食品及药物管理局(FDA)申请新药Ropeginterferon alfa-2b-njft(简称Ropeg,即P1101)新增适应症,新增适应症为原发性血小板过多症(ET),预计2026年取证,抢攻美国约15万ET病患市场,并将成为公司第二成长引擎。
-
《生医股》国邑*L608登美国风湿学会 首款居家治疗SSc-DU新药亮相
国邑*(6875)自主开发的吸入新药L608(微脂体-伊洛前列素)在2025年美国风湿学会年会(ACR 2025)上发表一期临床试验成果。本次数据不仅佐证了L608具备良好的安全性和耐受性,更重要的是,在关键的药物动力学(PK)指标上展现出突破性优势,为美国尚无核准疗法的系统性硬化症相关肢端溃疡(SSc-DU)市场开启先发契机。
-
《兴柜股》安基生技甘迺迪氏症新药AJ201 获美FDA快速审查认定
安基生技(7754)治疗甘迺迪氏症/脊髓延髓性肌肉萎缩症(Kennedy’s Disease 亦称Spinal and Bulbar Muscular Atrophy, SBMA)的AJ201,获美国食品药物管理局(FDA)授予快速审查认定。
-
安基罕病新药AJ201 获美国FDA授予快速审查认定
安基(7754)22日公告,旗下治疗甘迺迪氏症/脊髓延髓性肌肉萎缩症(SBMA)的AJ201,获美国FDA授予快速审查认定(Fast Track Designation, FTD)。该新药先前已获FDA与欧洲盟EMA孤儿药认定(Orphan Drug Designations, ODD)。
-
华安泡泡龙新药申请美国二期临床 攻24亿美元商机
华安(6657)22日公告,自主开发的遗传性表皮分解性水疱症(Epidermolysis Bullosa, EB,俗称「泡泡龙」)乳膏新药F703EB,向美国FDA提交二期临床试验申请。由于EB目前尚无根本疗法,F703EB挟卓越的机转优势,可望作为泡泡龙患者加速伤口癒合的第一线药物,抢攻全球24亿美元的罕病药物商机。
-
《生医股》华安泡泡龙新药 申请美国二期临床
华安(6657)今(22)日公告,自主开发的遗传性表皮分解性水疱症(Epidermolysis Bullosa, EB,俗称泡泡龙)乳膏新药F703EB,向美国食品药物管理局(FDA)提交二期临床试验申请。由于EB目前尚无根本疗法,F703EB挟卓越的机转优势,可望作为泡泡龙患者加速伤口癒合的第一线药物,抢攻全球24亿美元的罕病药物商机。
-
安成生技忧郁症新药 送件FDA
安成生技(6610)旗下口服前驱药物新药NORA520用于治疗产后忧郁症(PPD)及重度忧郁症(MDD),于9月与美国FDA完成Type C会议,并于10月16日接获官方会议纪录。FDA同意若第二期临床结果符合预期,可作为枢纽试验送件,显示该药临床开发迈入关键阶段。
-
安基新药AJ201登上世界肌肉学会年会 脊髓延髓肌肉萎缩症治疗现曙光
安基生技(7754)13日表示,旗下治疗脊髓延髓肌肉萎缩症(SBMA,又称甘迺迪氏症)的创新疗法AJ201,于世界肌肉学会(World Muscle Society, WMS)会中发表转译医学与临床试验最新成果,并以临床二期试验(Phase 2a)结果入选为今年仅有的七项「最新临床突破研究」(Late-Breaking Oral Abstract)之一,获邀进行口头报告,成为全场焦点。
-
视航生医乾眼症眼药水 迈大步
视航生物医学(7759)日前公告该公司SHJ002眼药水用于乾眼症治疗,三期临床试验已完成美国FDA的人体临床试验审查申请(IND申请)送件,预计于2026年展开试验收案。
-
安成生技 明年迎授权金高峰期
安成生技(6610)受惠产后忧郁症口服新药NORA520,将于第四季公布二期解盲数据,而治疗单纯型表皮分解性水疱症(EBS)软膏新药AC-203,也规画明年第一季进行2/3期中分析,安成生技董事长吴怡君指出,二新药陆续见成果,将带动公司明年进入授权金高峰期。
-
首家日本生技股在台挂牌 瑞格拚明年上半年登兴柜
首家日本生技股在台挂牌!瑞格拚明年上半年登录兴柜,营运长杨思圣22日表示,旗下用于GvHD(移植物抗宿主病)免疫调节新药RGI-2001,已在美国七家顶尖医学中心完成人体临床二期(Phase IIb)试验,2026年可望正式启动三期临床试验。该新药二b期试验成果已正式刊登于国际血液学顶尖期刊《Blood》。
-
《产业》瑞格新药RGI-2001 2b期临床成果刊登Blood期刊
开发免疫性疾病和癌症新型疗法的瑞格国际生技宣布,创新免疫调节新药RGI-2001已在美国七家顶尖医学中心完成临床2b期试验,并于早期的1/2a期试验展现优异的安全性与初步疗效。
-
《兴柜股》仁新斯特格LBS-008试验完成 Q4公布DRAGON结果
仁新(6696)子公司Belite宣布完成旗下LBS-008(Tinlarebant)口服新药针对青少年斯特格病变(STGD1)关键临床三期试验DRAGON,最后一位受试者已完成最后访视,Belite预计于2025年第4季公布DRAGON顶线数据结果(Top-line results),并规划于2026年上半年提交新药查验登记申请(NDA)。
-
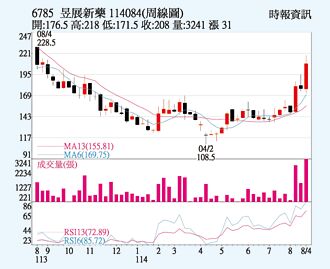
昱展 新药拓市报捷
昱展(6785)受惠授权伙伴Indivior将资源聚焦在戒毒瘾药物NDV-60001(ALA-1000),已在10个收案中心启动多重剂量药物动力学的收案,明年正式启动三期临床试验,8月以来吸引买盘进驻,22日以208元作收,上涨3.48%,成交量1,106张。技术面均线、KD指标均为多头排列,后市有利。
-
《生医股》共信-KY新药布局加速 PTS302打入中国200家医院
共信-KY(6617)今(30)日召开法说会,总经理林懋元指出,下半年营运将聚焦两大主轴:一是持续扩大旗下新药PTS302在中国市场的市占率,二是加速推动全球取证布局。此外,公司也积极推进临床试验中新药,当中用于治疗恶性犬类黑色素瘤的新药,预计最快第三季可望取得台湾药证,将成为公司首度跨足宠物癌症药物领域的重要里程碑。
-
新旭用APN-1607 打造早筛利器
国内药厂也迎头赶上失智症检测和新药开发,其中主打神经退化性疾病精准诊断的新旭生医(APN LifeSciences),获得雅诗兰黛家族创立的「阿兹海默症药物开发基金会(ADDF)」策略性投资,其正子造影显影剂「18F-APN-1607 (Florzolotau[18FJ])」可追踪脑部Tau蛋白病变,以精准诊断阿兹海默症及进行性核上性麻痹(PSP)等Tau蛋白相关的疾病,该产品已在全球收案超过4,000例,建立大规模临床影像资料库,并启动全球多中心临床试验,包括美国阿兹海默症临床二期以及获得美国食品药物管理局(FDA)「孤儿药与快速通道认定(Orphan Drug and Fast Track Designations)」之PSP行动障碍诊断临床三期。
-
新旭生医 获ADDF策略性投资
台湾生技研发能量被世界看见。新旭生医宣布,获得「阿兹海默症药物发展基金会(ADDF)」的策略性投资。ADDF是由美妆巨头雅诗兰黛家族创立,该投资将加速新旭APN 1607的开发。
-
《兴柜股》因华生技口服胆道癌孤儿新药 启动全球三期临床试验
因华生技(4172)宣布开发口服胆道癌孤儿新药 D07001-Softgel正式进入全球第三期关键性临床试验,并与美国知名CRO(临床研究机构)携手合作,该CRO将执行美国FDA药证申请的全球临床试验,预计收案约240名受试者,力拼2025年底美国试验地区,首位受试者入组,2026年底可收完期中解盲病人数。
-
《产业》丽宝新药携手阳明交大 运用AI技术加速抗癌药开发
丽宝新药与国立阳明交通大学今(1)日签署产学合作备忘录(MOU),共同启动「人工智慧导向之新药开发计画」。丽宝新药总经理刘朝瀚(Dr. Henry Liu)表示,这次双方强强联手,目标将AI运用在临床药物开发上,以缩短试验时程并提升药物测试的效率与准确度,同时也加速药证的取得。